Hintergrund: Bulk-Kristallisation von Proteinen zur Aufarbeitung und Formulierung
Biotechnologisch durch Zellkulturen oder GMO’s hergestellte Proteine werden üblicherweise durch chromatographische Verfahren und Filtration aus der Fermentationsbrühe abgetrennt und in mehreren Schritten gereinigt (downstream processing). Teure Chromatographiesäulen und Membranen sowie lange Zykluszeiten im Downstreaming verursachen dabei oft mehr als die Hälfte der Kosten des gesamten Herstellungsprozesses. Im Zuge des wachsenden Bedarfs an therapeutisch wirksamen Proteinen (z.B. Antikörper, Insulin) und industriellen Enzymen steht die Kostenreduzierung des downstream processing im Fokus der aktuellen pharmazeutischen und biotechnologischen Forschung. Als kostengünstige Alternative zur Chromatographie gilt die Kristallisation von Proteinen, welche ebenfalls eine hochselektive Technologie darstellt und zudem leichter in größere Maßstäbe skalierbar ist.
Kristallin formulierte Proteine haben weiterhin den Vorteil, dass sie bei Raumtemperatur eine hohe Lagerstabilität aufweisen und gute Handhabungseigenschaften besitzen. Proteine könnten also, wie bei zahlreichen weiteren pharmazeutischen Wirkstoffen (APIs) schon längst der Fall, durch Kristallisation der Darreichung in Tablettenform oder als Kapseln zugänglich gemacht werden.
Spezielle Herausforderungen
Proteinkristalle sind durchsetzt von Poren und Kanälen, durch welche ständig die umgebende Mutterlauge diffundiert. So enthalten sie bis zu 60 % Flüssigkeit in den Hohlräumen des Kristalls sowie gebunden als Hydratwasser. Die daraus resultierende Empfindlichkeit gegenüber mechanischen Beanspruchungen ist bei der Auslegung von Proteinkristallisationsprozessen besonders zu berücksichtigen. Weiterhin besitzen Proteine eine hohe pH- und Temperatursensitivität, was bei der Wahl des Kristallisationsprozesses von entscheidender Bedeutung ist.
Stand der Technik
Die Kristallisation eines Proteins wird üblicherweise durch Zugabe eines löslichkeitsmindernden Präzipitanten (z.B. Salz, PEG, Ethanol,…) zur Proteinlösung herbeigeführt. Neben dem ökologischen Nachteil dieser sogenannten „salting-out“, „drowning-out“ oder „anti-solvent“- Kristallisationsprozesse ist zudem ein nachfolgender Rückgewinnungsschritt notwendig. Weiterhin kann es beim Vermischen der beiden Eduktlösungen zu Übersättigungsspitzen an der Grenzfläche der beiden Komponenten kommen, welche zu feinem Kristallisat oder gar zur Denaturierung des Proteins führen können. Die Kristallausbeute der Prozesse ist durch die Löslichkeit der Edukte stark begrenzt.
Geeignete Alternativen, welche die vorstehenden Nachteile überwinden können, sind in der Literatur bislang kaum beschrieben.
Projekt: Technische Proteinkristallisation zur Aufreinigung, Stabilisierung und Formulierung pharmazeutisch aktiver Proteine
Im Rahmen dieses BMBF-geförderten Projektes werden anhand des Modellproteins Lysozym im Milliliter- bis Liter-Maßstab verschiedene Kristallisationsprozesse („salting-out“, Verdampfungskristallisation, Kühlungskristallisation) auf ihre Eignung für die technische Proteinkristallisation untersucht und geeignete Prozessstrategien entwickelt. Hauptaugenmerk liegt dabei nebst der Erhaltung der biologischen Aktivität des Proteins auf der Erzielung hoher Kristallausbeuten, der gewünschten Kristallmorphologie (z.B. stäbchenförmige Kristalle, isometrische Kristalle, Nadeln) und der gewünschten Kristallgrößenverteilung. Im Fokus aktueller Untersuchungen steht dabei die Verdampfungskristallisation, welche für anorganische Substanzen weit verbreitet ist, für Proteine bislang aber nicht untersucht wurde. Durch Verdampfung im Vakuum werden moderate Siedetemperaturen (20-40°C) gewährleistet, sodass das Protein nicht zerstört wird. Mit Lysozym konnte gezeigt werden, dass der Prozess ohne zusätzliches Präzipitant funktioniert und sehr hohe Kristallausbeuten erzielt werden können. Die biologische Aktivität des Enzyms bleibt im untersuchten Siedebereich erhalten. In Abhängigkeit von Ionenstärke und Siedetemperatur wurden 3 verschiedene Kristallmorphologien beobachtet (s. Abb.1-3). Laufende Experimente beschäftigen sich mit der Kinetik der Keimbildung und des Kristallwachstums mit dem Ziel, die Kristallgrößenverteilung geeignet beeinflussen zu können.
 |
 |
| Abb.1: Isometrischer Habitus | Abb.2: stäbchenförmiger Habitus (REM-Aufnahme) |
 |
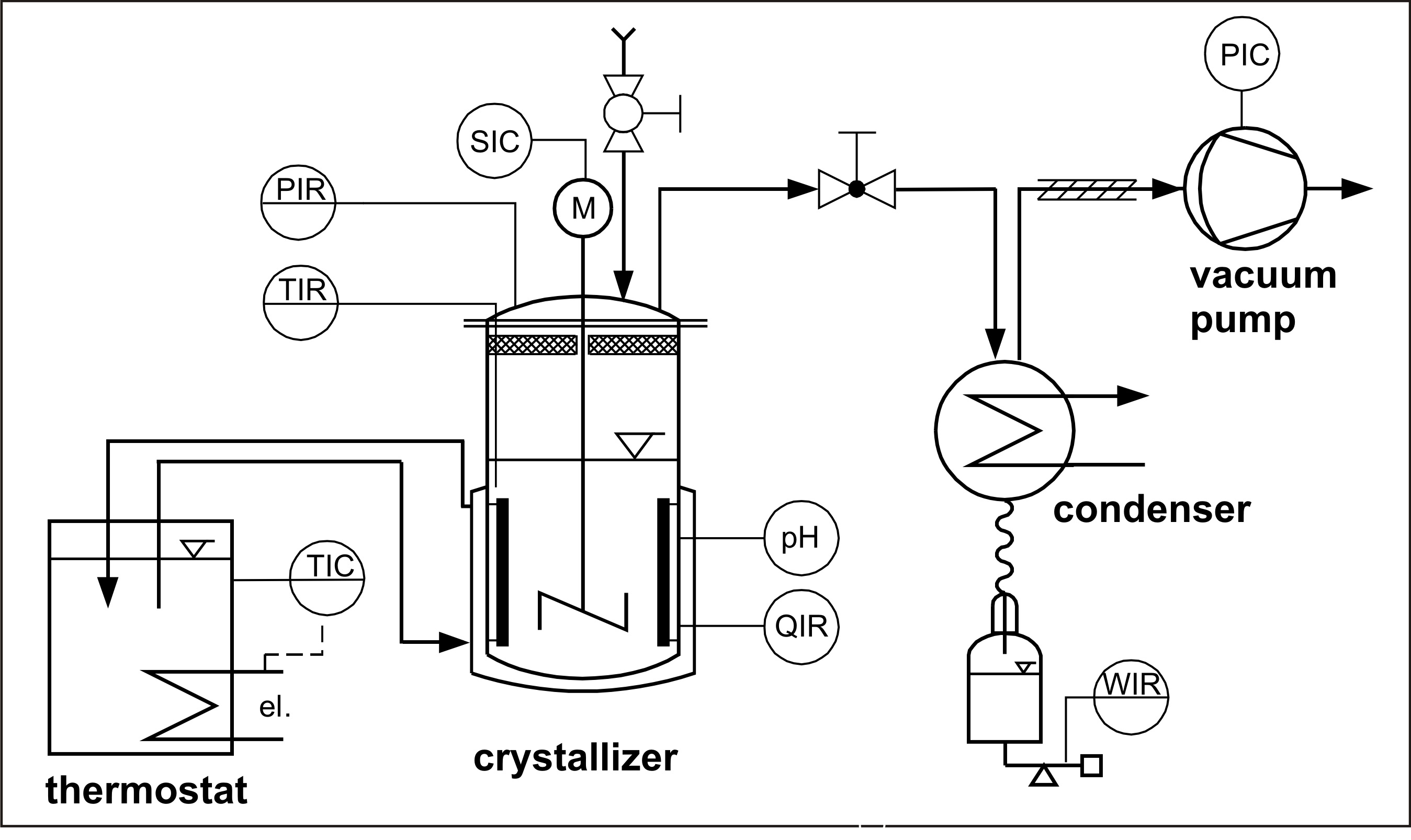 |
| Abb.3: Nadelförmige Kristalle | Abb.4: R&I-Fließbild Verdampfungskristallisation |

